解説編
抗HIV 療法の開始時期と薬剤選択
Last updated: 2022-09-29
初回抗HIV療法の開始時期
1. 日和見疾患を発症していない場合
強力な多剤併用療法(Highly Active Antiretroviral Therapy; いわゆる「ART」)が可能となった1996年頃からしばらくの間は、体内からHIVを排除することを目標として、早期に治療を導入することが推奨されていた(“Hit HIV early and hard”)。しかし、1) 長期にわたり良好なウィルス抑制状態を維持した場合でも治療中断によりウィルスが再度血中に出現すること、2) これは感染後早期に潜伏感染細胞(リザーバー)が生ずるためであり、現在の治療戦略で体内からHIVを排除することは不可能であること、などがその後の数年で明らかとなった。これを受けて2000年以降頃から、薬剤の長期毒性やQOLの低下、薬剤耐性獲得の危険を考慮して、CD4数200~350/μLとなるまで治療開始を待つ戦略(“Wait and see”)へとシフトする事になった。
しかし、エイズ発症の危険性がそれほど高くないと考えられるCD4数200/μL以上であっても、未治療あるいは治療中断の患者では、治療を行っている患者と比較して、動脈硬化性疾患やAIDS指標疾患に含まれない悪性腫瘍、認知機能障害などの様々な疾患が増加し、全死亡も増加することがその後の検討で明らかとなった(SMART試験1)、NA-ACCORD試験2))。これら非AIDS合併症は、免疫不全に加え持続的ウィルス血症に伴う慢性炎症を反映したものと考えられている。これらの病態に関する新たな知見に加え、抗HIV薬の効果と安全性、服薬の簡便性の向上もあり、2012年以降は「免疫不全に対して」ではなく「ウィルス血症のコントロールのために」抗HIV療法の早期導入が推奨されるに至った(表1)。感染者に対する早期抗HIV療法導入が未感染パートナーへのHIV感染リスクを低下させることも実証され(HPTN 052試験3)、PARTNER試験4))、早期治療の流れは加速した。2011年時点では多くの先進国のガイドラインがCD4数350~500/µLでの治療開始を推奨していたが、2012年以降の米国DHHSガイドラインは、(CD4数により推奨度に差はあるものの)CD4数に関わらず全例を抗HIV療法開始の適応としている。
抗HIV治療の開始時期の目安
(厚生労働省研究班 抗HIV治療ガイドライン, 2022年3月)
・CD4数に関わらずすべてのHIV感染者に抗HIV治療の開始を推奨する(AI)。
・治療開始にあたっては、服薬遵守の重要性を教育することや医療費減免のための社会資源の活用方法などについても詳しく説明しておかなければならない。早期の治療開始が推奨される近年においてはこれらの点への対応が以前にも増して重要となっている。
2. 日和見感染症を発症している場合
エイズ指標疾患、あるいはそれに準ずる日和見疾患を発症した症例は基本的に全例が抗HIV療法導入の適応となるが、適切な抗HIV療法開始時期については議論がある。早期に開始した場合、細胞性免疫能の早期回復による利益が期待されるが、薬剤の副作用や相互作用、免疫再構築症候群の問題が生じうる。結核に関しては、DHHSガイドラインでは、結核治療開始後8週間以内に抗HIV療法を開始すること、特に200/µL未満の場合には、結核治療開始後2~4週間以内に抗HIV療法を開始することを推奨している。ニューモシスチス肺炎・クリプトコッカス髄膜炎・細菌感染症の282例を対象に行われたACTG 5164試験5)では、14日以内の抗HIV療法開始により抗HIV療法の有効性を減ずることなくAIDS発症・死亡の危険を低下させたとの結果が得られ、これを受けて抗HIV療法開始時期が早期化する流れにある。ただしクリプトコッカス髄膜炎に関しては、2004年の報告により早すぎるART開始はIRISを介した過剰免疫により、有意に死亡率を上昇させる結果となっていた6)。
当施設においては、特異的な治療法が存在しない日和見疾患(進行性多巣性白質脳症等)や悪性リンパ腫合併例では可及的速やかな抗HIV療法開始、特異的治療が存在する日和見疾患の場合には初期治療による状態安定を待っての抗HIV療法導入を行っている。
日和見疾患発症後の適切なART開始については、常に最新のDHHSガイドライン等を確認した上で、疾患の重症度とIRIS発症による生命予後の悪化のリスクを勘案して、個別に判断されるべきである。
3. 急性HIV感染症
急性HIV感染症に対しても抗HIV療法の早期導入が推奨されているが、身体障害者手帳取得の問題もあり、症例ごとの判断が必要である。ただし、全身状態不良例や脳炎症状を呈する例に対しては、(慢性感染症としてではなく)予後改善を目的として、重症急性ウイルス感染症の原因に対する特異的治療としての抗HIV療法を積極的に導入すべきである。
薬剤選択
1. 初回治療
初回治療の場合、ガイドラインで推奨されている組み合わせであれば、どれを選択しても通常は良好なウィルス抑制効果が得られる。抗HIV療法の目標は、検出感度未満にウィルスを抑制「し続ける」ことであり、これを達成できるか否かは、良好な服薬アドヒアランスを維持できるかにかかっている。服薬継続の困難さに関わる因子として、各薬剤の制限事項(1回の服用錠剤数、食後内服の必要性、錠剤の大きさなど)、自覚的・他覚的な有害事象が重要であり、薬物相互作用にも配慮が必要である。推奨される組み合わせの中から、各症例の特徴に最も合致すると思われる組み合わせを選択する。2022年9月時点の日米のガイドラインを参考に、日本人に対して推奨される初回治療薬の組み合わせの概略、および薬剤選択の際に参考となる各推奨薬剤の特徴を表1・表2にまとめた。
米国DHHSガイドラインは日本のもの(通常年1回)より頻繁にアップデートされる傾向があり、最新動向に関してはこちらが参考にされる場合が多い。日本と米国で推奨に差がある部分については、通常日本側のガイドラインに理由が明記されており、参考となる。
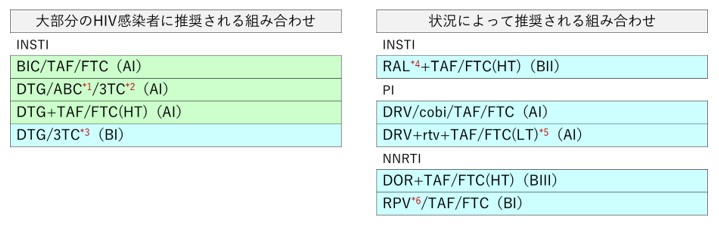
表1 日本人に対する初回治療の際に主に推奨される薬剤
(厚生労働省研究班 抗HIV治療ガイドライン, 2022年3月)
*1 HLA B*5701を有する患者(日本人では稀)ではABCの過敏症に注意を要する。ABC投与により心筋梗塞の発症リスクが高まるという報告がある。
*2 DTG/ABC/3TCはB型肝炎の合併がない患者にのみ推奨。
*3 DTG/3TCはB型肝炎の合併がなく、血中HIV-RNA量が50万コピー/mL未満、薬剤耐性検査で3TC, DTGに耐性のない患者にのみ推奨。
*4 RALはRAL 600mg錠の2錠(1200mg)を1日1回内服か、RAL400mg1錠を1日2回内服が可能。
*5 ブースター(cobi,あるいはrtv)を併用する組合せであるため。
*6 RPVは血中HIV-RNA量が10万コピー/mL未満の患者にのみ推奨。RPVはプロトンポンプ阻害剤内服者には使用しない。
注意1) RAL 400mg錠以外はすべてQD(1日1回)。 RAL 600mg錠は、1200mgを1日1回。
注意2) cobiやrtvはCYP阻害作用を有するので、 薬物相互作用に注意が必要(詳細は添付文書を参照)。 rtvはブースターとして少量を併用。
注意3) 配合剤が入手困難な場合は個別の薬剤の組み合わせでもよい。
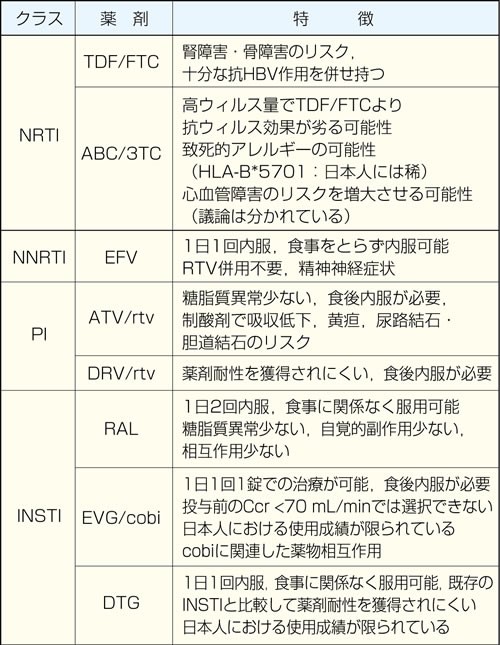
表2 初回治療の選択肢となる各薬剤の特徴
サルベージ治療
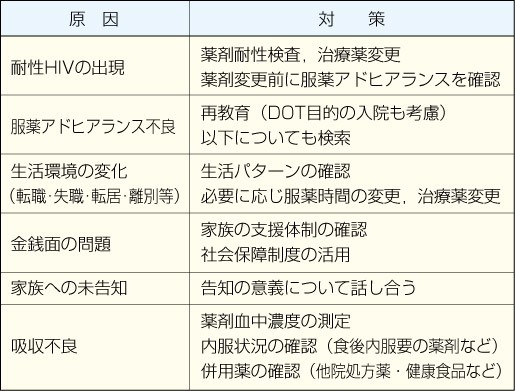
治療失敗の原因は必ずしも薬剤耐性とは限らない。服薬アドヒアランスが不良な状況で治療薬を変更しても、再び治療失敗に終わる可能性がある。失敗の原因(表3)を明らかにし、是正可能なものは是正した上で、必要があれば最適な治療薬の組み合わせに変更する。治療変更にあたっては、有効と考えられる薬剤を少なくとも2種類、可能なら3種類以上同時に開始することが重要である。
なお、薬剤耐性検査のうち、通常行われるgenotype assayでは、検査時点で投与されていない薬剤に対する耐性変異を検出できない場合がある。薬剤耐性検査の結果に加え、過去の治療(失敗)歴を詳細に分析することが必要である。
表3 治療失敗の原因と対策
ガイドライン
厚生労働省科学研究費補助金エイズ対策研究事業 抗HIV治療ガイドライン https://hiv-guidelines.jp/
日本エイズ学会 HIV感染症治療委員会 HIV感染症 治療の手引き http://www.hivjp.org/
米国DHHSガイドライン https://hivinfo.nih.gov/
欧州エイズ臨床学会ガイドライン https://www.eacsociety.org/guidelines/eacs-guidelines/
文献
1)Strategies for Management of Antiretroviral Therapy (SMART) Study Group, El-Sadr WM, et al. CD4+ count-guided interruption of antiretroviral treatment. N Engl J Med. 2006 Nov 30; 355(22): 2283-96.
2)Kitahata MM, et al. Effect of Early versus Deferred Antiretroviral Therapy for HIV on Survival. N Engl J Med 2009;360(18):1815-1826.
3)Cohen MS, et al. Antiretroviral Therapy for the Prevention of HIV-1 Transmission. N Engl J Med 2016;375:830-839.
4)Rodger AJ, et al. Risk of HIV transmission through condomless sex in serodifferent gay couples with the HIV-positive partner taking suppressive antiretroviral therapy (PARTNER): final results of a multicentre, prospective, observational study. Lancet 2019;393:2428-2438.
5)Zolopa AR, et al. Early Antiretroviral Therapy Reduces AIDS Progression/Death in Individuals with Acute Opportunistic Infections: A Multicenter Randomized Strategy Trial. PLoS One 2009;4(5):e5575.
6)Boulware DR, et al. Timing of Antiretroviral Therapy after Diagnosis of Cryptococcal Meningitis. N Engl J Med 2014;370:2487-2798.
著作権について
当サイト内のコンテンツ(文章・資料・画像・音声等)の著作権は、特に記載のない限り、国立国際医療センターエイズ治療・研究開発センターまたは第三者が保有します。営利、非営利を問わず、当サイトの内容を許可なく複製、転載、販売などに二次利用することを禁じます。