日和見疾患の診断・治療
HOME > 日和見疾患の診断・治療 > 結核
結核
Last updated: 2022-09-29
注意点
・CD4数の低い症例では、肺外結核が多く、播種性非結核性抗酸菌症や悪性リンパ腫との鑑別は困難である。
・治療は、非HIV感染者と大きく異なることはないが、リファマイシン系薬剤と抗HIV薬の間には、薬剤相互作用が多く、使用できない薬剤や投与量調整が必要な薬剤が多数存在する。
病原体
Mycobacterium tuberculosisの空気感染による。非HIV感染者にくらべHIV感染者はCD4数に関わらず結核を発症するリスクが高い。さらにHIVと結核の合併は相互に病状を進行させる。
臨床像
CD4数>350/µLでは非HIV患者と同様の臨床像をしめすことが多い(肺限局が多く、胸部X線で上肺野の散布・空洞陰影)。CD4数<200/µLでは典型的な肺結核所見は認めにくくなり、縦隔リンパ節腫脹、粟粒結核、肺外結核が多くみられる(写真1)。更にCD4<50/µLでは胸膜炎、心外膜炎、髄膜炎を発症することもある。感染臓器により症状が異なり、肺外結核の場合には、発熱や体重減少などの非特異的症状を呈する場合も多いため、臨床的に診断することは、極めて困難である。また、画像による他疾患との鑑別 (播種性NTM症、リンパ腫やカポジ肉腫などの悪性腫瘍) も容易ではなく、穿刺や生検などの侵襲的な検査が必要な場合が多い。
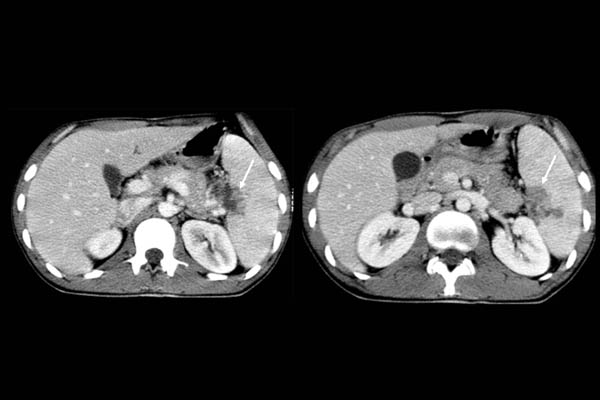
写真1 25 歳、男性CD4 41/µL
ニューモシスチス肺炎でAIDS 発症し治療終了後に発熱と左季肋部痛を主訴に 脾門部結核を発症。 ツベルクリン反応、喀痰の塗沫・抗酸菌培養全て陰性。
診断
喀痰や生検検体の培養検査もしくは拡散増幅検査 (PCR法) で、M. tuberculosis を同定することにより、診断する。HIV感染者では、M. tuberculosis 以外の非結核性抗酸菌 (NTM) による感染症の頻度も高いことから、結核感染が疑われる場合においても菌種の同定を行ってから治療を開始することが原則である。やむなく治療的診断目的で、抗結核薬を開始する場合もあるが、治療開始前に、採取可能な検体の微生物学的・組織学的検査を提出しなければならない。
a)喀痰検査・・・チール・ニールセン染色、オーラミン染色を行うとともに、培養検査・PCR検査を行う。塗抹陽性であっても、重度免疫不全症例では非結核性抗酸菌症の可能性もある。抗酸菌塗抹検査で陽性の場合には、必ず、PCR 検査で結核菌か否かを同定する。また、塗抹検査の結果のみから、慌てて結核病棟へ隔離してはならない。
また、HIV合併結核では耐性結核のリスクが高い (特に外国籍の患者) ことが知られているため、必ず培養を行い、後に抗結核剤の感受性が判明するよう努める。
b)胸部X線・・・免疫不全の進行に伴い非典型所見(肺野の浸潤影、著明な縦隔リンパ節腫大など)を呈する。胸部単純X線では所見に乏しい排菌陽性例も経験される。臨床的に、結核症が強く疑われる場合、または、IGRA (Interferon gamma release assay) 陽性例に対する活動性結核の除外には、CT撮影を積極的に検討する。
c)Interferon gamma release assays: IGRAs(QFT, T-SPOT)・・・活動性結核の診断は、病原体の同定 (培養・病理・核酸の同定など) を以て、行われなければならない。QFTやT-SPOTなどのIGRAsでの陽性結果は「結核感染」または「結核既感染」を示すものであり、活動性結核の診断には、有用ではない。
d) 生検・・・肺外結核の診断は、感染臓器を穿刺または摘出して採取された検体で、病原体を同定することで、行われる。既に肺結核症の診断が確定している症例での肺外病変については、他の疾患との鑑別が必要でない限りは、行う必要はない。結核性リンパ節炎であっても、細胞性免疫不全を反映し、生検病理組織における乾酪性肉芽腫などの所見は見られないため、HE染色のみによる結核感染の除外は出来ない。そのため、侵襲的検査で採取された検体に対して、抗酸菌塗抹検査や培養検査などの微生物学的検査を、必ず行うことが重要である。また、病理検査前に、リンパ腫や HHV-8 関連悪性腫瘍、播種性真菌症などを鑑別することは困難であるため、免疫染色 (EBER-ISH, HHV-8, etc.) や真菌を標的とした染色法 (Grocott’s methenamine silver 染色, Periodic Acid Schiff 染色, etc.) を、組み合わせて行う。
治療
非HIV患者のregimenに準ずる。INH (イソニアジド) 300mg+RFP (リファンピシン) 450mg+EB (エタンブトール) 750mg(+最初の2ヶ月間PZA (ピラジナミド) 1.2~1.5g )/日を6~9ヶ月間行う。また、髄膜炎、骨組織への浸潤や膿瘍形成している肺外結核では、より長期の治療も検討する。日本国内の結核菌では、耐性結核の頻度は高くないが、国外での感染が疑われる症例では、感受性検査の結果により、適宜処方を調整する必要があるため、培養検査で菌株を取得しておくことが、治療成功のためのポイントとなる。抗HIV療法 (ART) を開始する場合、リファマイシン系薬剤と抗HIV薬 (特に、プロテアーゼ阻害薬と一部のインテグラーゼ阻害薬) には強い相互作用があるため、用量を調整する必要がある(「part1.参考図表 抗酸菌治療薬と抗HIV薬併用時の投与法」http://www.acc.ncgm.go.jp/medics/treatment/handbook/part1/1-05.htmlを参照)。
ARTの開始時期については、一般的には抗結核治療を先行し、その後にARTを開始することが多い。これは、多数の薬剤を同時に開始することで副作用が出現した場合、原因薬剤の判別が困難となることが予想されることと、ART開始後の免疫再構築症候群(IRIS)(写真2)のリスクが高いためである。 一方、海外のガイドラインでは、他の日和見感染症発症を抑制するためには、結核診断から早期に ART を開始することが推奨されている。例えば、米国CDCガイドラインでは結核性髄膜炎を除き、CD4< 50/µLでは抗結核治療開始後2週間以内のART導入、またそれ以外では結核治療開始後2ヶ月以内のART導入が推奨されている。結核性髄膜炎を伴う場合のART 導入時期については、定まった方法はないが、抗結核薬開始から 2-8週間程度期間を空けてから、ART を導入することが、推奨されている。
上記のような状況で、国内施設での ART 開始時期に関する定まった見解はないが、当院(ACC)では、抗結核薬開始から 2-4 週以上の期間を置いて、抗結核薬の有害事象発生を確認した後、ART を開始している症例が多い。結核性髄膜炎を発症した症例に関しては、それ以上の期間をおいて、ARTを開始する場合が多く、個々の症例での検討が必要である。
免疫再構築症候群 (IRIS) は、ART 開始後に出現する新規の発熱やリンパ節腫脹 (unmasking IRIS)、あるいは、もともとあった病変の増悪 (paradoxical IRIS) という形で起こる。結核症では、診断時に発熱以外の症状を伴わない症例が多く、ART開始後に発熱を来たす場合、paradoxical IRISと薬剤熱との鑑別は難しい場合が多く、発疹の有無や免疫反応の増強を示すリンパ節増大などの所見を参考に判断する。一方、薬剤熱では抗結核薬投与開始10-14 日程度で発症することが多く、paradoxical IRIS の場合にはART開始2週間前後、多くは1ヶ月以内に起こることが多いため、各薬剤の開始後からの期間なども参考に、発熱の鑑別診断を行う。
IRIS の程度は、症例により異なり、未治療で自然軽快するものから、激烈でステロイド投与が必要な症例まで幅広い臨床像を呈する。一時的・短期間 (おおよそ数週から1か月以内) のステロイド投与を必要とする症例はあるものの、ART を中断しなければならないことは、ほとんど経験しない。IRIS は免疫の回復に伴って引き起こされる病原体への反応であり、臓器障害の程度が軽いと見込まれる場合には、IRISに対する治療は不要である。全例にステロイド投与が必要ではない。IRIS に対するステロイド投与可否を議論する場合、どの臓器に対する IRIS が起こっているか、IRIS による炎症が致死的または回復不能な後遺症をもたらす可能性が高いのか (例えば、結核性髄膜炎の IRIS など) を考慮し、一時的な免疫抑制によって、障害臓器の炎症を取り除く必要があるかを、個々の症例で評価する。安易な免疫抑制剤投与は、当該疾患の治癒を遅らせてしまうのみならず、他の日和見感染症発症・増悪リスクを高めてしまう。
ステロイドを投与する場合の用量や投与期間に、定められた方法はない。ガイドラインでは、プレドニゾロン 1.5mg/day 2週間の後、 0.75mg/day を2週間投与する方法が、表記されている。当科ではプレドニンで0.5-1mg/kg/dayよりスタートし、以後は3-5日ずつ熱型や臓器障害をみながら漸減することが多い。多くの症例は、このような数週から1か月程度のステロイド投与が奏効するものの、結核性髄膜炎など、致死的となる臓器病変を伴うIRIS症例では、より慎重な減量方法も考慮される。当院では、結核性髄膜炎でIRISと判断した場合、画像や髄液検査により、炎症の程度を評価しつつ、数か月間かけて、慎重にステロイド減量を行っている。
IRIS は、免疫反応であり、個々の症例により、その臓器障害と免疫反応の強さ、緊急性が異なる。致死的な臓器障害に注意を払いつつも、漫然と免疫抑制状態を継続することのないよう、留意されたい。
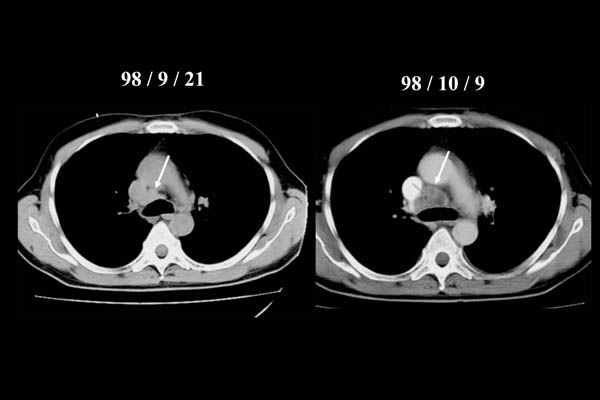
写真2 48歳、男性:1998年6月、ニューモシスチス肺炎でAIDS を発症。ST合剤による3週間の治療後にARTを開始。8月下旬に右S6に結節陰出現し、気管支内視鏡検査にて結核と診断されたため、HREZ による抗結核療法を開始した(CD4 91/µL)。9 月下旬より再び発熱、さらに10月には 肺門縦隔リンパ節腫脹も認め(CD4 202/µL)、ART による免疫再構築症候群と診断した。食道や気管への瘻孔形成が懸念されたため、ARTの一時中断を要した。
予防等
活動性結核の治療後の2次予防は不要である。一方、潜在性結核 (Latent Tuberculotic infection: LTbI) と診断した症例では、抗結核薬の投与を行い、活動性結核発症を予防することが、推奨されている。
潜在性結核 (LTbI) の診断と発症予防
結核菌暴露既往の有無に関わらず、全てのHIV診断例に対する IGRAs検査が推奨されており、LTbI 診断例へは活動性結核発症予防のため、抗結核薬が投与される。
潜在性結核の診断は、①IGRA陽性であること、かつ、②臨床的・画像的に活動性結核が否定できること、である。特に、②の活動性結核の除外は、極めて重要であり、活動性結核が存在するにもかかわらず、潜在性結核に対する抗結核薬投与は、不十分な治療による結核菌の耐性誘導が懸念される。海外では、発熱や喀痰などの結核症を疑う所見がないことに加え、胸部単純写真で肺結核が除外できれば、潜在性結核の診断となる。一方、国内の医療施設では、比較的容易にCT検査が実施可能であることから、我々の施設で、偶発的もしくはスクリーニングで、IGRA 陽性が判明した場合には、胸腹部CT により臓器病変がないか (活動性結核が存在しないか) を確かめた上で、潜在性結核の診断を行っている。
潜在性結核の治療について、過去には、イソニアジドの単剤6か月間投与が推奨されていたが、2剤併用による3か月の短期治療 (イソニアジド+リファンピシンなど) の有用性と安全性が示されていることから1~3)、米国のガイドラインでは2剤レジメンが推奨されている 4)。しかし、リファンピシンの代わりにリファブチンを用いた研究がないこと、リファンピシンと併用可能な抗HIV薬は極めて限定されることなどから、現段階では、HIV感染者における潜在性結核の治療について、定まった見解はない。リファンピシンと抗HIV薬の薬物相互作用を念頭に置き、最新の情報に注意を払いつつ、治療を選択する必要がある。
参考文献)
1)Rivero A, Lopez-Cortes L, Castillo R, et al. [Randomized clinical trial investigating three chemoprophylaxis regimens for latent tuberculosis infection in HIV-infected patients]. Enferm Infecc Microbiol Clin. 2007;25(5):305-310.
2)Johnson JL, Okwera A, Hom DL, et al. Duration of efficacy of treatment of latent tuberculosis infection in HIV-infected adults. AIDS. 2001;15(16):2137-2147.
3)Whalen CC, Johnson JL, Okwera A, et al. A trial of three regimens to prevent tuberculosis in Ugandan adults infected with the human immunodeficiency virus. Uganda-Case Western Reserve University Research Collaboration. N Engl J Med. 1997;337(12):801-808.
4)Guidelines for the Prevention and Treatment of Opportunistic Infections in Adults and Adolescents with HIV, Updated in Feb. 17, 2022
著作権について
当サイト内のコンテンツ(文章・資料・画像・音声等)の著作権は、特に記載のない限り、国立国際医療センターエイズ治療・研究開発センターまたは第三者が保有します。営利、非営利を問わず、当サイトの内容を許可なく複製、転載、販売などに二次利用することを禁じます。
